- ការសិក្សារបស់ CDC ស្តីពីការត្រួតពិនិត្យសុវត្ថិភាពនៃកម្រិតបន្ថែមនៃវ៉ាក់សាំង COVID-19
- អ្វីដែលត្រូវបានគេដឹងរួចទៅហើយអំពី the booster shot?
- ក្នុងចំណោមអ្នកចូលរួមក្នុងការសាកល្បងព្យាបាល Pfizer-BioNTech ចំនួន 306 នាក់ ប្រតិកម្មមិនល្អបន្ទាប់ពីចាក់ថ្នាំ 3 គឺស្រដៀងទៅនឹងអ្នកក្រោយដូស 2 ។
អ្វីដែលត្រូវបានបន្ថែមដោយរបាយការណ៍នេះ។ បាញ់លេខ ៣ ចេញដោយ CDC ថ្ងៃនេះ?
ក្នុងអំឡុងពេលថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 ក្នុងចំណោមអ្នកចុះឈ្មោះ v-safe ចំនួន 12,591 នាក់ ដែលបានបញ្ចប់ការស្ទង់មតិពិនិត្យសុខភាព បន្ទាប់ពីការចាក់វ៉ាក់សាំង mRNA COVID-3 ទាំង 19 ដូស 79.4% និង 74.1% បានរាយការណ៍ពីប្រតិកម្មក្នុងតំបន់ ឬជាប្រព័ន្ធរៀងៗខ្លួន បន្ទាប់ពី កម្រិតទីបី; 77.6% និង 76.5% បានរាយការណ៍ពីប្រតិកម្មក្នុងតំបន់ ឬជាប្រព័ន្ធបន្ទាប់ពីចាក់លើកទី XNUMX រៀងគ្នា។
តើអ្វីទៅជាផលប៉ះពាល់សម្រាប់ការអនុវត្តសុខភាពសាធារណៈ?
របាយការណ៍ស្ម័គ្រចិត្តទៅ v-safe បានរកឃើញថាមិនមានគំរូនៃប្រតិកម្មមិនល្អដែលមិននឹកស្មានដល់បន្ទាប់ពីការចាក់វ៉ាក់សាំង COVID-19 បន្ថែម។ CDC នឹងបន្តតាមដានសុវត្ថិភាពវ៉ាក់សាំង រួមទាំងការចាក់បន្ថែម COVID-19 ផងដែរ។
នៅថ្ងៃទី 12 ខែសីហា ឆ្នាំ 2021 រដ្ឋបាលចំណីអាហារ និងឱសថ (FDA) បានធ្វើវិសោធនកម្មការអនុញ្ញាតប្រើប្រាស់ក្នុងគ្រាអាសន្ន (EUAs) សម្រាប់វ៉ាក់សាំង Pfizer-BioNTech និង Moderna COVID-19 ដើម្បីអនុញ្ញាតការគ្រប់គ្រងកម្រិតថ្នាំបន្ថែមមួយបន្ទាប់ពីការបញ្ចប់នៃស៊េរីវ៉ាក់សាំងបឋមដល់អ្នកដែលមានសិទ្ធិទទួលបាន។ លក្ខខណ្ឌភាពស៊ាំចុះខ្សោយកម្រិតមធ្យមទៅធ្ងន់ធ្ងរ (1,2) នៅថ្ងៃទី 22 ខែកញ្ញា ឆ្នាំ 2021 FDA បានអនុញ្ញាតឲ្យចាក់វ៉ាក់សាំង Pfizer-BioNTech មួយបន្ថែមទៀត ≥6 ខែបន្ទាប់ពីការបញ្ចប់នៃស៊េរីបឋមក្នុងចំណោមមនុស្សដែលមានអាយុលើសពី 65 ឆ្នាំ ដែលមានហានិភ័យខ្ពស់សម្រាប់ COVID-19 ធ្ងន់ធ្ងរ ឬដែលការប៉ះពាល់ផ្នែកការងារ ឬស្ថាប័នដាក់ពួកគេនៅ ហានិភ័យខ្ពស់សម្រាប់ COVID-19 (1) លទ្ធផលពីការសាកល្បងព្យាបាលដំណាក់កាលទី 3 ដែលធ្វើឡើងដោយ Pfizer-BioNTech ដែលរួមបញ្ចូលមនុស្សចំនួន 306 នាក់ដែលមានអាយុពី 18-55 ឆ្នាំ បានបង្ហាញថា ប្រតិកម្មមិនល្អបន្ទាប់ពីការទទួលថ្នាំលើកទី 5 គ្រប់គ្រង 8-2 ខែបន្ទាប់ពីការបញ្ចប់ការចាក់វ៉ាក់សាំង mRNA បឋម 2 ដូសគឺស្រដៀងគ្នាទៅនឹង ដែលត្រូវបានរាយការណ៍បន្ទាប់ពីការទទួលថ្នាំ XNUMX; ប្រតិកម្មមិនល្អទាំងនេះរួមមានកន្លែងចាក់ថ្នាំកម្រិតស្រាលទៅមធ្យម និងប្រតិកម្មជាប្រព័ន្ធ (3) CDC បានបង្កើត v-safe ដែលជាប្រព័ន្ធឃ្លាំមើលសុវត្ថិភាពផ្អែកលើស្មាតហ្វូនដោយស្ម័គ្រចិត្ត ដើម្បីផ្តល់ព័ត៌មានអំពីប្រតិកម្មមិនល្អបន្ទាប់ពីការចាក់វ៉ាក់សាំង COVID-19 ។
ស្របពេលជាមួយនឹងការអនុញ្ញាតកម្រិតថ្នាំបន្ថែមសម្រាប់អ្នកដែលមានលក្ខខណ្ឌការពារភាពស៊ាំ វេទិកា v-safe ត្រូវបានធ្វើបច្ចុប្បន្នភាពដើម្បីឱ្យអ្នកចុះឈ្មោះបញ្ចូលព័ត៌មានអំពីកម្រិតបន្ថែមនៃវ៉ាក់សាំង COVID-19 ដែលទទួលបាន។ ក្នុងអំឡុងពេលថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 អ្នកចុះឈ្មោះដែលមានសុវត្ថិភាព v-safe សរុបចំនួន 22,191 នាក់បានរាយការណ៍ថាបានទទួលការចាក់វ៉ាក់សាំង COVID-19 បន្ថែមមួយ។ ភាគច្រើន (97.6%) បានរាយការណ៍ពីស៊េរីចាក់វ៉ាក់សាំង mRNA បឋម 2 ដូស បន្តដោយការចាក់លើកទីបីនៃវ៉ាក់សាំងដូចគ្នា។ ក្នុងចំណោមអ្នកដែលបានបញ្ចប់ការស្ទង់មតិពិនិត្យសុខភាពសម្រាប់ថ្នាំទាំង 3 ដូស (12,591; 58.1%), 79.4% និង 74.1% បានរាយការណ៍ពីប្រតិកម្មក្នុងតំបន់ ឬជាប្រព័ន្ធ រៀងគ្នាបន្ទាប់ពីចាក់ថ្នាំ 3 ធៀបនឹង 77.6% និង 76.5% ដែលបានរាយការណ៍តាមមូលដ្ឋាន ឬជាប្រព័ន្ធ។ ប្រតិកម្មរៀងៗខ្លួនបន្ទាប់ពីចាក់ថ្នាំទី 2។ ការរកឃើញដំបូងទាំងនេះបង្ហាញថាមិនមានគំរូនៃប្រតិកម្មមិនល្អដែលមិននឹកស្មានដល់បន្ទាប់ពីការចាក់វ៉ាក់សាំង COVID-19 បន្ថែម។ ភាគច្រើននៃប្រតិកម្មមិនល្អទាំងនេះគឺស្រាល ឬមធ្យម។ CDC នឹងបន្តតាមដានសុវត្ថិភាពវ៉ាក់សាំង រួមទាំងសុវត្ថិភាពនៃកម្រិតបន្ថែមនៃវ៉ាក់សាំង COVID-19 និងផ្តល់ទិន្នន័យដើម្បីណែនាំការណែនាំអំពីវ៉ាក់សាំង និងការពារសុខភាពសាធារណៈ។
V-safe គឺជាប្រព័ន្ធឃ្លាំមើលសុវត្ថិភាពរបស់សហរដ្ឋអាមេរិកដែលមានមូលដ្ឋានលើស្មាតហ្វូនដោយស្ម័គ្រចិត្ត។ អ្នកទទួលថ្នាំបង្ការដែលមានសិទ្ធិទទួលបានផលិតផលវ៉ាក់សាំងដែលមានការអនុញ្ញាត ឬមានអាជ្ញាប័ណ្ណអាចចុះឈ្មោះនៅក្នុង v-safe ។ វេទិកា v-safe អនុញ្ញាតឱ្យអ្នកចុះឈ្មោះដែលមានស្រាប់រាយការណ៍ពីការទទួលបានវ៉ាក់សាំង COVID-19 បន្ថែម និងអ្នកចុះឈ្មោះថ្មីដើម្បីបញ្ចូលព័ត៌មានអំពីគ្រប់ដូសនៃវ៉ាក់សាំង COVID-19 ដែលទទួលបាន។ ការស្ទង់មតិសុខភាព V-safe ត្រូវបានផ្ញើក្នុងកំឡុងថ្ងៃ 0-7 បន្ទាប់ពីការចាក់វ៉ាក់សាំងនីមួយៗ ហើយរួមបញ្ចូលសំណួរអំពីកន្លែងចាក់ថ្នាំក្នុងតំបន់ និងប្រតិកម្មជាប្រព័ន្ធ និងផលប៉ះពាល់សុខភាព។* ការស្ទង់មតិត្រូវបានផ្ញើសម្រាប់កម្រិតថ្នាំដែលបានបញ្ចូលថ្មីៗបំផុត។† សមាជិកបុគ្គលិកមកពីប្រព័ន្ធរាយការណ៍ពីព្រឹត្តិការណ៍អវិជ្ជមាននៃវ៉ាក់សាំង (VAERS) ទាក់ទងអ្នកចុះឈ្មោះដែលបង្ហាញថាការយកចិត្តទុកដាក់ខាងវេជ្ជសាស្ត្រត្រូវបានស្វែងរកបន្ទាប់ពីការចាក់វ៉ាក់សាំង និងលើកទឹកចិត្ត ឬសម្របសម្រួលការបញ្ចប់របាយការណ៍ VAERS ប្រសិនបើបានបញ្ជាក់។§
ក្នុងចំណោមអ្នកចុះឈ្មោះដែលមានសុវត្ថិភាព v-safe ដែលបានរាយការណ៍ពីការទទួលថ្នាំបង្ការ COVID-19 បន្ថែមក្នុងកំឡុងថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 ទិន្នន័យប្រជាសាស្រ្ត ប្រតិកម្មក្នុងតំបន់ និងជាប្រព័ន្ធ និងផលប៉ះពាល់សុខភាពដែលបានរាយការណ៍ក្នុងកំឡុងថ្ងៃ 0-7 ត្រូវបានពិពណ៌នាដោយគំរូនៃការទទួលថ្នាំបង្ការ (ឧ។ ក្រុមហ៊ុនផលិតវ៉ាក់សាំងដែលបានទទួលសម្រាប់ដូសនីមួយៗ)។ អ្នកដែលបានរាយការណ៍ថាទទួលបានស៊េរីបឋមពីក្រុមហ៊ុនផលិតផ្សេងៗគ្នា ឬក្រុមហ៊ុនផលិតដែលមិនស្គាល់ ឬមិនមាននៅក្នុងសហរដ្ឋអាមេរិក ឬវ៉ាក់សាំង 2 ដូស បន្ទាប់ពីបានទទួលវ៉ាក់សាំងតែមួយដូស Janssen (Johnson & Johnson) (150) ត្រូវបានដកចេញពីការវិភាគ នៃប្រតិកម្មមិនល្អបន្ទាប់ពីទទួលបានកម្រិតបន្ថែម។
ពេលវេលាដែលបានកន្លងផុតទៅពីការបញ្ចប់នៃស៊េរីចាក់ថ្នាំបង្ការបឋមរហូតដល់ការទទួលថ្នាំបន្ថែមត្រូវបានពិពណ៌នាតាមលំនាំនៃការចាក់វ៉ាក់សាំង។ ទម្រង់នៃព្រឹត្តិការណ៍មិនល្អបន្ទាប់ពីដូស 2 និង 3 ត្រូវបានប្រៀបធៀបសម្រាប់អ្នកចុះឈ្មោះដែលបានទទួលវ៉ាក់សាំង mRNA ពីក្រុមហ៊ុនផលិតដូចគ្នាសម្រាប់ 3 ដូស។¶ កម្មវិធី SAS (កំណែ 9.4; វិទ្យាស្ថាន SAS) ត្រូវបានប្រើដើម្បីធ្វើការវិភាគទាំងអស់។ សកម្មភាពឃ្លាំមើលទាំងនេះត្រូវបានត្រួតពិនិត្យដោយ CDC និងបានធ្វើឡើងស្របតាមច្បាប់សហព័ន្ធជាធរមាន និងគោលនយោបាយ CDC ។**
ក្នុងអំឡុងពេលថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 អ្នកចុះឈ្មោះដែលមានសុវត្ថិភាព v-safe សរុបចំនួន 22,191 នាក់បានរាយការណ៍ថាបានទទួលការចាក់វ៉ាក់សាំង COVID-19 បន្ថែម បន្ទាប់ពីបានបញ្ចប់ស៊េរីបឋម (តារាង 1) ក្នុងចំណោមនោះ ១៤.០៤៨ (៦៣.៣%) ជាស្ត្រី ហើយប្រមាណ ៣០% ម្នាក់ៗមានអាយុពី ១៨-៤៩ ឆ្នាំ ៥០-៦៤ និង ៦៥-៧៤ ឆ្នាំ។
អ្នកចុះឈ្មោះភាគច្រើន (21,662; 97.6%) បានរាយការណ៍ថាពួកគេបានទទួលដូសទីបីពីក្រុមហ៊ុនផលិតដូចគ្នាទៅនឹងស៊េរីវ៉ាក់សាំង mRNA ចម្បងរបស់ពួកគេ រួមទាំង 98.6% នៃអ្នកទទួល Moderna និង 98.2% នៃអ្នកទទួល Pfizer-BioNTech ។ អ្នកចុះឈ្មោះតិចតួច (341; 1.5%) បានរាយការណ៍ពីស៊េរីវ៉ាក់សាំង mRNA បឋមដែលបន្តដោយការចាក់បន្ថែមនៃវ៉ាក់សាំង mRNA ពីក្រុមហ៊ុនផលិតផ្សេងគ្នា ដូសនៃវ៉ាក់សាំង Janssen បន្ទាប់ពីបានទទួលស៊េរីវ៉ាក់សាំង mRNA បឋម (10; 0.05%) ឬបន្ថែម កម្រិតថ្នាំវ៉ាក់សាំង COVID-19 ពីក្រុមហ៊ុនផលិតណាមួយបន្ទាប់ពីវ៉ាក់សាំង Janssen (178; 0.8%)។
ក្នុងចំណោមអ្នកចុះឈ្មោះ 22,191 v-safe ចន្លោះពេលជាមធ្យមពីការបញ្ចប់នៃស៊េរីការចាក់វ៉ាក់សាំងបឋម COVID-19 ដល់ការទទួលថ្នាំបន្ថែមគឺ 182 ថ្ងៃ (ចន្លោះចន្លោះ [IQR] = 160–202 ថ្ងៃ) (តារាង 2) ក្នុងចំណោមអ្នកដែលទទួលបានវ៉ាក់សាំង Janssen ចំនួន 2 ដូស ចន្លោះពេលជាមធ្យមរវាងការចាក់គឺខ្លីជាង (84 ថ្ងៃ; IQR = 16-136 ថ្ងៃ) ។
ប្រតិកម្មក្នុងតំបន់ (16,615; 74.9%) និងជាប្រព័ន្ធ (15,503; 69.9%) ត្រូវបានគេរាយការណ៍ជាញឹកញាប់ក្នុងអំឡុងពេលសប្តាហ៍បន្ទាប់ពីការចាក់វ៉ាក់សាំង COVID-19 បន្ថែម ដែលភាគច្រើនជាទូទៅបំផុតនៅថ្ងៃបន្ទាប់ពីការទទួលថ្នាំបង្ការ។ ប្រតិកម្មដែលត្រូវបានរាយការណ៍ជាញឹកញាប់គឺការឈឺចាប់នៅកន្លែងចាក់ថ្នាំ (15,761; 71.0%) អស់កម្លាំង (12,429; 56.0%) និងឈឺក្បាល (9,636; 43.4%) ។
ក្នុងចំណោមអ្នកទទួលថ្នាំបន្ថែមចំនួន 22,191 នាក់ សរុបចំនួន 7,067 (31.8%) បានរាយការណ៍ពីផលប៉ះពាល់សុខភាព ហើយប្រហែល 28.3% (6,287) បានរាយការណ៍ថា ពួកគេមិនអាចធ្វើសកម្មភាពប្រចាំថ្ងៃធម្មតាបានទេ ដែលភាគច្រើនបំផុតនៅថ្ងៃបន្ទាប់ពីការទទួលថ្នាំបង្ការ។ ការថែទាំវេជ្ជសាស្រ្តត្រូវបានស្វែងរកដោយអ្នកចុះឈ្មោះចំនួន 401 (1.8%) ហើយដប់បី (0.1%) ត្រូវបានបញ្ជូនទៅមន្ទីរពេទ្យ។ ហេតុផលសម្រាប់ការទទួលបានការថែទាំវេជ្ជសាស្រ្ត ឬការចូលមន្ទីរពេទ្យមិនត្រូវបានកំណត់អត្តសញ្ញាណនៅក្នុងការស្ទង់មតិ v-safe; ទោះយ៉ាងណាក៏ដោយ អ្នកចុះឈ្មោះដែលបង្ហាញថាការយកចិត្តទុកដាក់ខាងវេជ្ជសាស្ត្រត្រូវបានស្វែងរកបន្ទាប់ពីការទទួលថ្នាំបង្ការត្រូវបានទាក់ទងដោយបុគ្គលិក VAERS និងលើកទឹកចិត្តឱ្យបំពេញរបាយការណ៍ VAERS ។
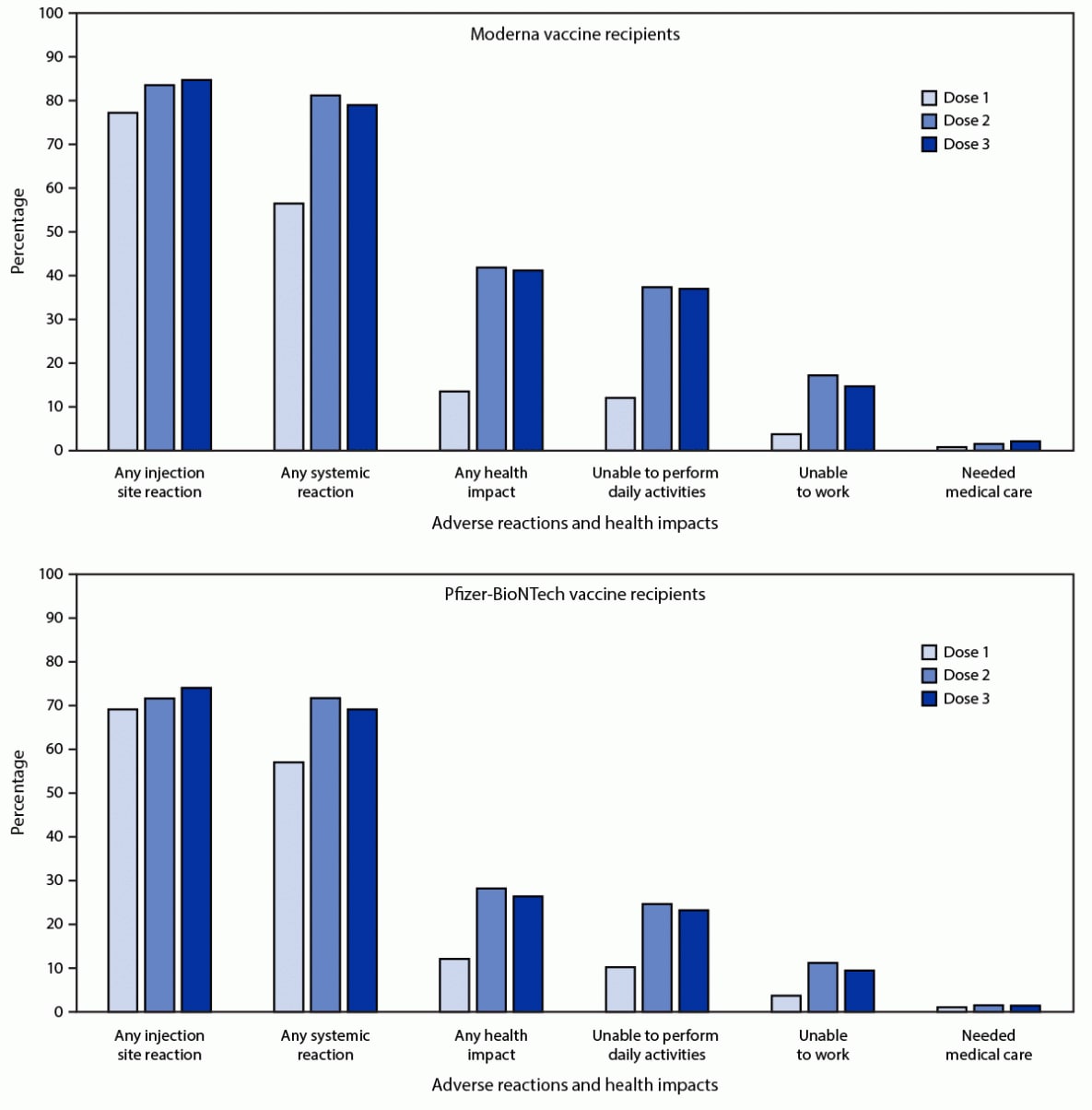
ក្នុងចំណោមអ្នកចុះឈ្មោះដែលមានសុវត្ថិភាព 21,658 នាក់ដែលបានទទួលវ៉ាក់សាំង mRNA ដូចគ្នាសម្រាប់ទាំង 3 ដូស 12,591 (58.1%) បានបញ្ចប់ការស្ទង់មតិពិនិត្យសុខភាពយ៉ាងហោចណាស់មួយនៅថ្ងៃទី 0-7 បន្ទាប់ពីការចាក់ទាំង 3 ដង។ 79.4% និង 74.1% បានរាយការណ៍ពីប្រតិកម្មក្នុងតំបន់ ឬជាប្រព័ន្ធរៀងៗខ្លួន បន្ទាប់ពីកិតទី 3 ធៀបនឹង 77.6% និង 76.5% ដែលបានរាយការណ៍ពីប្រតិកម្មក្នុងតំបន់ ឬជាប្រព័ន្ធ រៀងគ្នាបន្ទាប់ពីកិត 2។ ក្នុងចំណោមអ្នកចុះឈ្មោះដែលទទួលបាន 3 ដូសនៃ Moderna (6,283) ក្នុងស្រុក ប្រតិកម្មត្រូវបានគេរាយការណ៍កាន់តែញឹកញាប់បន្ទាប់ពីដូសទី 3 ជាងដូសទី 2 (5,323; 84.7% និង 5,249; 83.5%; p-value = 0.03) (តួលេខ) ប្រតិកម្មជាប្រព័ន្ធត្រូវបានគេរាយការណ៍តិចតួចបន្ទាប់ពីកិតទី 3 ជាងដូសទី 2 (4,963; 79.0% និង 5,105; 81.3%; p-value <0.001)។
ក្នុងចំណោមអ្នកចុះឈ្មោះដែលទទួលបាន 3 ដូសនៃ Pfizer-BioNTech (6,308) ប្រតិកម្មក្នុងតំបន់ត្រូវបានរាយការណ៍ញឹកញាប់ជាងបន្ទាប់ពីចាក់ថ្នាំ 3 ជាងដូស 2 (4,674; 74.1% និង 4,523; 71.7%; p-value < 0.001) ។ ប្រតិកម្មជាប្រព័ន្ធត្រូវបានគេរាយការណ៍តិចតួចបន្ទាប់ពីដូសទី 3 ជាងដូសទី 2 (4,363; 69.2% និង 4,524; 71.7%; p-value <0.001)។ ក្នុងចំណោមអ្នកដែលបានរាយការណ៍ពីការឈឺចាប់បន្ទាប់ពីចាក់ថ្នាំវ៉ាក់សាំង mRNA លើកទី 3 ប្រតិកម្មភាគច្រើនគឺស្រាល (4,909; 51.4%) ឬមធ្យម (4,000; 41.9%) ។ ការឈឺចាប់ធ្ងន់ធ្ងរ (កំណត់ថាជាការឈឺចាប់ដែលធ្វើឱ្យសកម្មភាពប្រចាំថ្ងៃពិបាក ឬមិនអាចទៅរួច) ត្រូវបានរាយការណ៍ដោយ 637 (6.7%) ។
ការពិភាក្សា
គិតត្រឹមថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 មនុស្សប្រមាណ 2.21 លាននាក់នៅសហរដ្ឋអាមេរិកបានទទួលវ៉ាក់សាំង COVID-19 បន្ថែម។†អឺរ៉ុប បន្ទាប់ពីបញ្ចប់ស៊េរីបឋម។ ចាប់ពីថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021 គ្មានគំរូនៃប្រតិកម្មមិនល្អត្រូវបានគេសង្កេតឃើញក្នុងចំនោមអ្នកចុះឈ្មោះដែលមានសុវត្ថិភាព 22,191 ដែលទទួលបានវ៉ាក់សាំងកូវីដ-19 កម្រិតបន្ថែម។ ប្រតិកម្មក្នុងមូលដ្ឋាន និងជាប្រព័ន្ធដែលត្រូវបានរាយការណ៍ភាគច្រើនគឺស្រាលទៅមធ្យម បណ្តោះអាសន្ន និងញឹកញាប់បំផុតដែលត្រូវបានរាយការណ៍នៅថ្ងៃបន្ទាប់ពីការទទួលថ្នាំបង្ការ។ អ្នកចុះឈ្មោះភាគច្រើនដែលបានទទួលដូសបន្ថែមបានរាយការណ៍ពីស៊េរីវ៉ាក់សាំង mRNA បឋមដែលបន្តដោយដូសទីបីពីក្រុមហ៊ុនផលិតដូចគ្នា។
ការសាកល្បងព្យាបាលរបស់ Pfizer-BioNTech ដែលរួមមានមនុស្សចំនួន 306 នាក់ដែលមានអាយុពី 18-55 ឆ្នាំ បានបង្ហាញថា ប្រតិកម្មបន្ទាប់ពីចាក់ថ្នាំ 3 គឺអាចប្រៀបធៀបទៅនឹងអ្នកដែលបានរាយការណ៍បន្ទាប់ពីដូស 2 (3) ទោះជាយ៉ាងណាក៏ដោយ ការវិភាគនៃទិន្នន័យសុវត្ថិភាព v-safe នេះបានរកឃើញថា ប្រតិកម្មក្នុងតំបន់គឺជារឿងធម្មតាជាងបន្តិច ហើយប្រតិកម្មជាប្រព័ន្ធគឺមិនសូវមានធម្មតាទេ បន្ទាប់ពីកម្រិតទី 3 នៃ Pfizer-BioNTech ។
គំរូនៃប្រតិកម្មមិនល្អដែលបានសង្កេតឃើញបន្ទាប់ពីចាក់ថ្នាំលើកទី 3 នៃវ៉ាក់សាំង Moderna ឬ Pfizer-BioNTech គឺស្របជាមួយនឹងប្រតិកម្មដែលបានពិពណ៌នាពីមុនបន្ទាប់ពីបានទទួលថ្នាំ 2
ចំនួនអ្នកចុះឈ្មោះដែលបង្ហាញថាពួកគេបានទទួលវ៉ាក់សាំង Janssen ចំនួន 2 ដូស ឬបានទទួលកម្រិតថ្នាំបន្ថែមរបស់ពួកគេពីក្រុមហ៊ុនផលិតខុសពីស៊េរីចម្បងរបស់ពួកគេគឺតូច ដោយកំណត់ការសន្និដ្ឋានណាមួយ។
ទិន្នន័យស្តីពីសុវត្ថិភាព ឬប្រសិទ្ធភាពនៃការចាក់វ៉ាក់សាំងជាមួយផលិតផលវ៉ាក់សាំង COVID-19 ពីក្រុមហ៊ុនផលិតផ្សេងៗគ្នាត្រូវបានកំណត់។ គណៈកម្មាធិការប្រឹក្សាស្តីពីការអនុវត្តការចាក់ថ្នាំបង្ការ (ACIP) ណែនាំថាអ្នកដែលមានលក្ខខណ្ឌការពារភាពស៊ាំពីកម្រិតមធ្យមទៅធ្ងន់ធ្ងរទទួលបានវ៉ាក់សាំង mRNA COVID-19 មួយដូសទីបីពីក្រុមហ៊ុនផលិតដូចគ្នាទៅនឹងស៊េរីចម្បងរបស់ពួកគេ។
ការណែនាំរបស់ CDC សម្រាប់កម្រិតថ្នាំបន្ថែមបច្ចុប្បន្នមិនរាប់បញ្ចូលអ្នកដែលទទួលបានវ៉ាក់សាំង Janssen ទេ។
ក្នុងអំឡុងពេលដែលគ្របដណ្តប់ដោយការសិក្សានេះ ការណែនាំរបស់ ACIP សម្រាប់កម្រិតបន្ថែមនៃវ៉ាក់សាំង COVID-19 ត្រូវបានកំណត់ចំពោះអ្នកដែលមានលក្ខខណ្ឌការពារភាពស៊ាំពីមធ្យមទៅធ្ងន់ធ្ងរដែលបានទទួល។
វ៉ាក់សាំង mRNA ចំនួន ២ ដូស។
ការសិក្សាមួយដែលធ្វើឡើងក្នុងចំណោមអ្នកជំងឺ hemodialysis នៃប្រព័ន្ធភាពស៊ាំបានរាយការណ៍ថា ប្រតិកម្មក្នុងតំបន់ និងជាប្រព័ន្ធបន្ទាប់ពីការចាក់ថ្នាំវ៉ាក់សាំង Pfizer-BioNTech កម្រិតទី 3 គឺស្រដៀងគ្នាទៅនឹងថ្នាំបន្ទាប់ពីចាក់ថ្នាំ 2 ។¶¶ របាយការណ៍ថ្មីៗនៃការឆ្លងចំពោះអ្នកទទួលថ្នាំបង្ការ និងការកើនឡើងនៃអត្រាប្រេវ៉ាឡង់នៃការឆ្លងមេរោគជាមួយនឹងវ៉ារ្យ៉ង់ B.1.617.2 (Delta) នៃ SARS-CoV-2 ដែលជាមេរោគដែលបង្កឱ្យកើតជំងឺកូវីដ-១៩ ក្នុងចំណោមអ្នកទទួលថ្នាំបង្ការប្រហែលជាបានជំរុញឱ្យមនុស្សមួយចំនួនស្វែងរក កម្រិតថ្នាំបន្ថែមក្រៅពីការណែនាំ។ ចន្លោះពេលជាមធ្យមចាប់ពីការបញ្ចប់ស៊េរីបឋមរហូតដល់ការទទួលថ្នាំបន្ថែមគឺប្រហែល 19 ខែ។ ដូច្នេះ អ្នកដែលផ្តល់អាទិភាពក្នុងអំឡុងពេលដាក់ឱ្យប្រើប្រាស់វ៉ាក់សាំង COVID-6 រួមទាំងបុគ្គលិកថែទាំសុខភាព និងមនុស្សចាស់អាចទទួលបានកម្រិតថ្នាំបន្ថែម។
ការរកឃើញនៅក្នុងរបាយការណ៍នេះគឺស្ថិតនៅក្រោមការកំណត់យ៉ាងហោចណាស់បួន។ ទីមួយ ការចុះឈ្មោះក្នុង v-safe គឺជាការស្ម័គ្រចិត្ត ហើយទំនងជាមិនមែនជាតំណាងនៃប្រជាជនអាមេរិកដែលទទួលថ្នាំបង្ការនោះទេ។ អ្នកចូលរួមភាគច្រើនបានកំណត់អត្តសញ្ញាណខ្លួនឯងថាជាជនជាតិស្បែកស និងមិនមែនជាជនជាតិអេស្ប៉ាញ។ ទីពីរ ក្នុងអំឡុងពេលនៃការសិក្សានេះ ការណែនាំកម្រិតថ្នាំបន្ថែមត្រូវបានកំណត់ចំពោះអ្នកដែលមានលក្ខខណ្ឌការពារភាពស៊ាំដែលបានបញ្ចប់ស៊េរីវ៉ាក់សាំងបឋម mRNA COVID-19 ។ ទោះយ៉ាងណាក៏ដោយ v-safe មិនរួមបញ្ចូលព័ត៌មានអំពីស្ថានភាពភាពស៊ាំទេ។
អ្នកទទួលថ្នាំបន្ថែមទំនងជារួមបញ្ចូលអ្នកដែលមាន និងគ្មានលក្ខខណ្ឌការពារភាពស៊ាំ។ ទីបី ទំនាក់ទំនងបុព្វហេតុរវាងវ៉ាក់សាំង និងព្រឹត្តិការណ៍អវិជ្ជមានធ្ងន់ធ្ងរដែលត្រូវបានរាយការណ៍បន្ទាប់ពីការទទួលថ្នាំបង្ការមិនអាចបង្កើតបានដោយប្រើទិន្នន័យសុវត្ថិភាព v-safe ។ ជាចុងក្រោយ ទិន្នន័យមិនគ្រប់គ្រាន់អាចរកបានដើម្បីកំណត់គំរូនៃប្រតិកម្មមិនល្អ បន្ទាប់ពីបានទទួលកម្រិតថ្នាំបន្ថែមពីក្រុមហ៊ុនផលិតខុសពីស៊េរីចម្បង ឬសម្រាប់វ៉ាក់សាំង Janssen ។
ការចាក់វ៉ាក់សាំង mRNA COVID-19 បន្ថែមមួយត្រូវបានណែនាំសម្រាប់អ្នកដែលមានលក្ខខណ្ឌភាពស៊ាំចុះខ្សោយពីមធ្យមទៅធ្ងន់ធ្ងរ (5).
CDC បានផ្តល់អនុសាសន៍ឱ្យចាក់វ៉ាក់សាំង Pfizer-BioNTech បន្ថែមទៀត ≥6 ខែបន្ទាប់ពីការបញ្ចប់នៃស៊េរីវ៉ាក់សាំងបឋមក្នុងចំណោមមនុស្សដែលមានអាយុលើសពី 65 ឆ្នាំ អ្នករស់នៅក្នុងកន្លែងថែទាំរយៈពេលវែង និងមនុស្សដែលមានអាយុពី 50-64 ឆ្នាំដែលមានលក្ខខណ្ឌសុខភាពមូលដ្ឋាន។ មនុស្សដែលមានអាយុពី 18-49 ឆ្នាំដែលមានលក្ខខណ្ឌសុខភាពមូលដ្ឋាន និងមនុស្សដែលមានអាយុពី 18-64 ឆ្នាំដែលមានហានិភ័យខ្ពស់សម្រាប់ការប៉ះពាល់ និងឆ្លងជំងឺកូវីដ-19 ដោយសារតែការកំណត់ពីការងារ ឬស្ថាប័នអាចទទួលបានកម្រិតថ្នាំបន្ថែមដោយផ្អែកលើអត្ថប្រយោជន៍ និងហានិភ័យផ្ទាល់ខ្លួនរបស់ពួកគេ។
ការវិភាគដំបូងនៃទិន្នន័យសុវត្ថិភាពពីអ្នកចុះឈ្មោះ > 22,000 v-safe បង្ហាញថាប្រតិកម្មក្នុងតំបន់ត្រូវបានកើនឡើងបន្តិច ហើយប្រតិកម្មជាប្រព័ន្ធត្រូវបានថយចុះបន្តិចបន្ទាប់ពីដូសទី 3 នៃ mRNA ជាងបន្ទាប់ពីដូស 2 ។
គ្មានគំរូដែលមិនរំពឹងទុកនៃប្រតិកម្មមិនល្អត្រូវបានគេកំណត់អត្តសញ្ញាណ; របាយការណ៍ទាំងនោះមានកម្រិតស្រាលទៅមធ្យម និងបណ្តោះអាសន្ន។ CDC នឹងបន្តតាមដានសុវត្ថិភាពនៃកម្រិតបន្ថែមនៃវ៉ាក់សាំង COVID-19។ ទិន្នន័យបន្ថែមអំពីប្រតិកម្មមិនល្អដែលទាក់ទងនឹងការរួមផ្សំគ្នានៃវ៉ាក់សាំង និងពេលវេលាចាប់តាំងពីការបញ្ចប់ស៊េរីបឋមនឹងមានសារៈសំខាន់ដើម្បីណែនាំការណែនាំអំពីសុខភាពសាធារណៈ។
| លក្ខណៈ | ទំនើប %† (n = ១០.៦០១) | Pfizer-BioNTech, %† (n = ១០.៦០១) | Janssen, %†, § (n = ១០.៦០១) | សរុប (N = ១.៤០៩.២១៨) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ដូស 3 Moderna (n = 10,453; 98.6%) | ដូស 3 Pfizer-BioNTech (n = 144; 1.4%) | ដូស 3 Janssen (n = 4; 0.04%) | ដូស 3 Pfizer-BioNTech (n = 11,209; 98.2%) | ដូស 3 Moderna (n = 197; 1.7%) | ដូស 3 Janssen (n = 6; 0.1%) | ដូស 2 Janssen (n = 48; 27.0%) | ដូស 2 Moderna (n = 64; 36.0%) | ដូស 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| ការរួមភេទ | ||||||||||
| ស្រី | 63.8 | 63.9 | 50.0 | 63.0 | 63.5 | 33.3 | 39.6 | 57.8 | 59.1 | 63.3 |
| បុរស | 35.1 | 34.0 | 50.0 | 36.1 | 36.0 | 66.7 | 60.4 | 42.2 | 40.9 | 35.7 |
| មិនស្គាល់ | 1.0 | 2.1 | 0 | 0.9 | 0.5 | 0 | 0 | 0 | 0 | 1.0 |
| ក្រុមអាយុ, ឆ្នាំ | ||||||||||
| 0-17 | 0.0 | 0.7 | 0.0 | 0.6 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.3 |
| 18-49 | 25.7 | 36.1 | 25.0 | 31.5 | 42.6 | 50.0 | 54.2 | 60.9 | 57.6 | 29.1 |
| 50-64 | 28.4 | 27.1 | 50.0 | 31.1 | 29.9 | 0.0 | 33.3 | 34.3 | 30.3 | 29.8 |
| 65-74 | 33.9 | 27.1 | 0.0 | 27.8 | 21.3 | 50.0 | 10.4 | 4.7 | 9.1 | 30.5 |
| 75-84 | 10.9 | 9.0 | 25.0 | 8.3 | 5.6 | 0.0 | 2.1 | 0.0 | 3.0 | 9.5 |
| ≥85 | 1.1 | 0.0 | 0.0 | 0.7 | 0.5 | 0.0 | 0.0 | 0.0 | 0.0 | 0.9 |
| ជនជាតិ | ||||||||||
| អ្នកនិយាយភាសាអេស្ប៉ាញ / ឡាតាំង | 8.0 | 15.3 | 0 | 8.2 | 5.6 | 0 | 25.0 | 6.3 | 10.6 | 8.2 |
| មិននិយាយភាសាអេស្ប៉ាញ/ឡាទីន | 87.7 | 81.9 | 100 | 87.6 | 90.9 | 100 | 54.2 | 89.1 | 89.4 | 87.6 |
| មិនស្គាល់ | 4.3 | 2.8 | 0 | 4.2 | 3.6 | 0 | 20.8 | 4.7 | 0 | 4.2 |
| ការប្រណាំង | ||||||||||
| AI/AN | 0.5 | 0.7 | 0 | 0.5 | 0.5 | 0 | 2.1 | 0 | 0 | 0.5 |
| អាស៊ី | 4.9 | 5.6 | 0 | 6.1 | 7.1 | 0 | 2.1 | 14.1 | 13.6 | 5.6 |
| ខ្មៅ | 5.6 | 3.5 | 0 | 6.2 | 1.5 | 16.7 | 6.3 | 6.3 | 9.1 | 5.9 |
| NHPI | 0.2 | 0 | 0 | 0.3 | 0.5 | 0 | 4.2 | 0 | 0 | 0.3 |
| ស | 82.6 | 82.6 | 100 | 80.4 | 85.8 | 66.7 | 56.3 | 71.9 | 69.7 | 81.4 |
| ពហុភាសា | 1.9 | 2.1 | 0 | 1.8 | 1.5 | 16.7 | 4.2 | 4.7 | 3.0 | 1.9 |
| ផ្សេងទៀត | 2.1 | 4.2 | 0 | 2.1 | 0.5 | 0 | 6.3 | 1.6 | 3.0 | 2.1 |
| មិនស្គាល់ | 2.3 | 1.4 | 0 | 2.5 | 2.5 | 0 | 18.8 | 1.6 | 1.5 | 2.4 |
អក្សរកាត់: AI/AN = ជនជាតិដើមអាមេរិក ឥណ្ឌា/អាឡាស្កា; NHPI = ជនជាតិដើមហាវ៉ៃ ឬអ្នកកោះប៉ាស៊ីហ្វិកផ្សេងទៀត។
* ភាគរយនៃអ្នកចុះឈ្មោះដែលបានបញ្ចប់ការស្ទង់មតិពិនិត្យសុខភាព v-safe យ៉ាងហោចណាស់មួយនៅថ្ងៃ 0-7 បន្ទាប់ពីការចាក់វ៉ាក់សាំង។
† ស៊េរីវ៉ាក់សាំងបឋម។
§ រាប់បញ្ចូលទាំងអ្នកដែលទទួលបានថ្នាំ Janssen បឋមមួយដូស និងវ៉ាក់សាំងបន្ថែម 1 ដូសពីក្រុមហ៊ុនផលិតដែលបានរាយបញ្ជី។
| ប្រតិកម្ម | ទំនើប %† (n = ១០.៦០១) | Pfizer-BioNTech, %† (n = ១០.៦០១) | Janssen, %†, § (n = ១០.៦០១) | សរុប (N = ១.៤០៩.២១៨) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ដូស 3 Moderna (n = 10,453; 98.6%) | ដូស 3 Pfizer-BioNTech (n = 144; 1.4%) | ដូស 3 Janssen (n = 4; 0.04%) | ដូស 3 Pfizer-BioNTech (n = 11,209; 98.2%) | ដូស 3 Moderna (n = 197; 1.7%) | ដូស 3 Janssen (n = 6; 0.1%) | ដូស 2 Janssen (n = 48; 27.0%) | ដូស 2 Moderna (n = 64; 36.0%) | ដូស 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| ថ្ងៃចាប់តាំងពីស៊េរីបឋម មធ្យម (IQR) | 182 (164 - 198) | 183 (161 - 204) | 173 (141 - 182) | 183 (157 - 209) | 186 (161 - 217) | 123 (113 - 182) | 84 (16 - 136) | 156 (140 - 164) | 150 (136 - 167) | 182 (160 - 202) |
| ប្រតិកម្មនៅកន្លែងចាក់ថ្នាំណាមួយ។ | 80.9 | 64.6 | 75.0 | 69.4 | 81.7 | 83.3 | 25.0 | 70.3 | 80.3 | 74.9 |
| រមាស់ | 20.0 | 11.8 | 0 | 8.4 | 10.2 | 16.7 | 10.4 | 6.3 | 7.6 | 13.9 |
| ឈឺចាប់ | 75.9 | 60.4 | 75.0 | 66.6 | 80.2 | 83.3 | 20.8 | 68.8 | 74.2 | 71.0 |
| ក្រហម | 25.2 | 8.3 | 0 | 9.8 | 20.8 | 16.7 | 6.3 | 7.8 | 12.1 | 17.1 |
| ហើម | 33.6 | 17.4 | 0 | 16.8 | 30.5 | 16.7 | 6.3 | 12.5 | 18.2 | 24.8 |
| ប្រតិកម្មប្រព័ន្ធណាមួយ។ | 75.2 | 59.7 | 50.0 | 65.1 | 76.1 | 100 | 31.3 | 68.8 | 63.6 | 69.9 |
| ឈឺពោះ | 8.4 | 3.5 | 0 | 6.4 | 8.1 | 16.7 | 4.2 | 3.1 | 6.1 | 7.3 |
| Myalgia | 49.8 | 29.2 | 0 | 36.3 | 49.2 | 50.0 | 20.8 | 45.3 | 33.3 | 42.7 |
| ញាក់ | 31.3 | 8.3 | 50.0 | 17.5 | 33.5 | 50.0 | 8.3 | 23.4 | 10.6 | 24.1 |
| រាគ | 9.9 | 7.6 | 0 | 9.0 | 9.6 | 16.7 | 8.3 | 6.3 | 9.1 | 9.4 |
| អស់កម្លាំង | 61.8 | 44.4 | 0 | 51.0 | 60.9 | 83.3 | 14.6 | 48.4 | 50.0 | 56.0 |
| ុន | 36.4 | 20.1 | 50.0 | 22.2 | 37.1 | 50.0 | 6.3 | 37.5 | 12.1 | 29.0 |
| ឈឺក្បាល | 49.0 | 31.1 | 0 | 38.4 | 49.7 | 83.3 | 18.8 | 35.9 | 40.9 | 43.4 |
| ឈឺសន្លាក់ | 33.0 | 18.8 | 0 | 23.0 | 31.0 | 33.3 | 16.7 | 20.3 | 19.7 | 27.7 |
| ចង្អោរ | 18.8 | 10.4 | 25.0 | 13.6 | 21.3 | 33.3 | 8.3 | 9.4 | 18.2 | 16.1 |
| កន្ទុយ | 2.3 | 0.7 | 0 | 1.9 | 2.5 | 0 | 4.2 | 1.6 | 1.5 | 2.1 |
| ក្អួត | 2.2 | 2.1 | 25.0 | 1.4 | 2.0 | 0 | 2.1 | 0 | 0 | 1.7 |
| ប៉ះពាល់សុខភាពណាមួយ។ | 39.2 | 19.4 | 0 | 25.2 | 39.1 | 33.3 | 16.7 | 28.1 | 24.2 | 31.8 |
| មិនអាចអនុវត្តសកម្មភាពប្រចាំថ្ងៃធម្មតាបានទេ។ | 35.2 | 18.1 | 0 | 22.1 | 33.0 | 33.3 | 10.4 | 25.0 | 15.2 | 28.3 |
| មិនអាចធ្វើការ ឬចូលរៀនបានឡើយ។ | 13.7 | 4.9 | 0 | 9.0 | 21.3 | 16.7 | 10.4 | 6.3 | 13.6 | 11.3 |
| ត្រូវការការថែទាំវេជ្ជសាស្រ្ត | 2.1 | 1.4 | 0 | 1.5 | 3.0 | 0 | 6.3 | 0 | 0 | 1.8 |
| Telehealth | 0.9 | 0.7 | 0 | 0.7 | 1.0 | 0 | 2.1 | 0 | 0 | 0.8 |
| គ្លីនិក | 0.7 | 0.7 | 0 | 0.6 | 0.5 | 0 | 4.2 | 0 | 0 | 0.6 |
| ដំណើរទស្សនកិច្ចបន្ទាន់ | 0.2 | 0 | 0 | 0.2 | 0 | 0 | 4.2 | 0 | 0 | 0.2 |
| មន្ទីរពេទ្យ | 0.05 | 0 | 0 | 0.1 | 0 | 0 | 0 | 0 | 0 | 0.1 |
កម្លាំង. ប្រតិកម្មមិនល្អ និងផលប៉ះពាល់សុខភាពដែលត្រូវបានរាយការណ៍ដោយអ្នកដែលទទួលបាន 3 ដូស* នៃ Moderna (N = 6,283) ឬវ៉ាក់សាំង Pfizer-BioNTech (N = 6,308) COVID-19 ហើយបានបញ្ចប់ការស្ទង់មតិពិនិត្យសុខភាព v-safe យ៉ាងហោចណាស់មួយនៅថ្ងៃ 0– 7 បន្ទាប់ពីដូសនីមួយៗ តាមចំនួនដូស — សហរដ្ឋអាមេរិក ថ្ងៃទី 12 ខែសីហា ដល់ថ្ងៃទី 19 ខែកញ្ញា ឆ្នាំ 2021
អ្វីដែលត្រូវយកចេញពីអត្ថបទនេះ៖
- Results from a phase 3 clinical trial conducted by Pfizer-BioNTech that included 306 persons aged 18–55 years showed that adverse reactions after receipt of a third dose administered 5–8 months after completion of a 2-dose primary mRNA vaccination series were similar to those reported after receipt of dose 2.
- Persons who reported receiving a primary series from different manufacturers or a manufacturer that was unknown or unavailable in the United States, or 2 doses of vaccine after receipt of a Janssen (Johnson &.
- On August 12, 2021, the Food and Drug Administration (FDA) amended Emergency Use Authorizations (EUAs) for the Pfizer-BioNTech and Moderna COVID-19 vaccines to authorize administration of an additional dose after completion of a primary vaccination series to eligible persons with moderate to severe immunocompromising conditions (1,2).






















